Infecciones causadas por hongos pueden provocar síntomas de Alzheimer
Estudios clínicos han mostrado que infecciones externas pueden invadir el cerebro
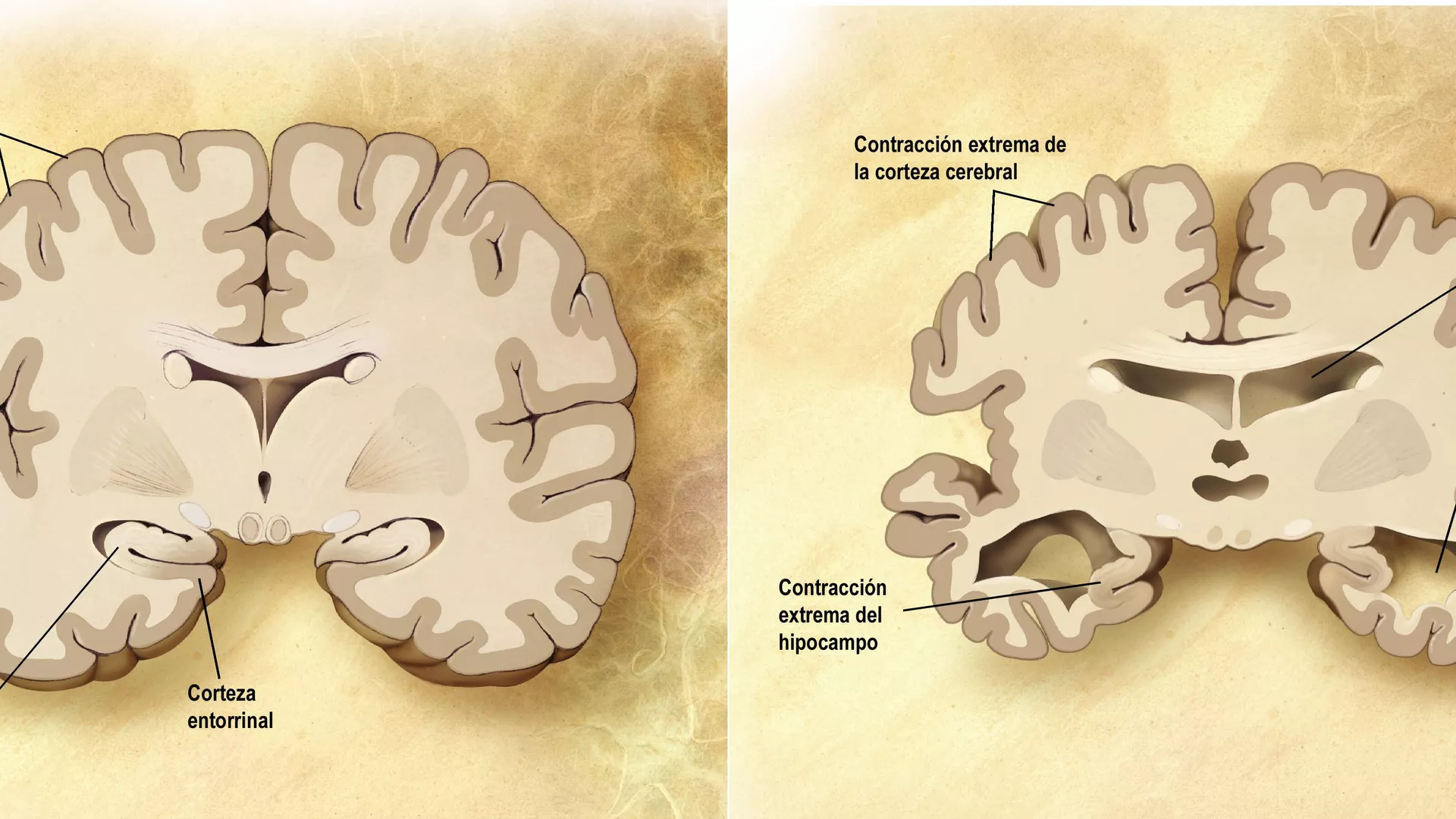
18/10/23.- Un grupo de científicos comprobó que un tipo común de hongos penetra en el cerebro de los mamíferos y provoca placas amiloides tóxicas como las asociadas a la enfermedad de Alzheimer. Los datos proceden de ratones, pero se sugiere que una característica clave de algunas enfermedades neurodegenerativas podría tener su origen fuera del cerebro, señala la agencia de noticias rusa, Sputnik.
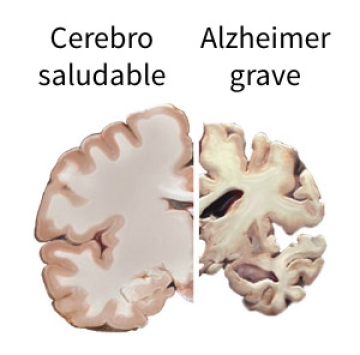
Los cúmulos de proteína amiloide que aparecen entre las neuronas, están estrechamente relacionados con la enfermedad de Alzheimer y, por lo general, se cree que son el resultado del estrés intrínseco o de la inflamación del cerebro.
En los últimos años, sin embargo, los científicos han detectado signos de un hongo común, conocido como Candida albicans, en las autopsias de cerebros de personas con alzhéimer y otros trastornos neurodegenerativos, como el párkinson. Esto lleva a algunos a argumentar que las infecciones externas pueden invadir el cerebro de los mamíferos y provocar una respuesta inmunitaria innata, que puede servir para destruir patógenos, pero que también provocaría síntomas parecidos a los del Alzheimer si va mal.
Esta semana se han publicado los resultados de un esperanzador ensayo en animales que podría arrojar más luz al respecto. En ratones se ha descubierto cómo el hongo Candida albicans penetra en el cerebro, activa 2 mecanismos distintos en las células cerebrales que favorecen su eliminación y genera péptidos similares al beta amiloide.
En 2019, el equipo liderado por expertos del Baylor College of Medicine en EEUU informó que la Candida albicans es capaz de producir cambios cerebrales muy similares a lo que se observa en este tipo de demencia. Encontró que los ratones infectados con este hongo mostraban alteraciones de la memoria, que se resolvían cuando se eliminaba. El estudio actual amplía ese trabajo para intentar comprender los mecanismos moleculares que se ponen en marcha.
"Nuestra primera pregunta fue: ¿cómo entra C. albicans en el cerebro? Descubrimos que C. albicans produce unas enzimas denominadas proteasas aspárticas secretadas (Saps) que rompen la barrera hematoencefálica, lo que permite al hongo acceder al cerebro, donde causa daños", explica en nota de prensa el Dr. Yifan Wu, primer autor y científico postdoctoral en pediatría que trabaja en el laboratorio de Corry.
2 mecanismos neuroinmunes para acabar con el intruso
Cristina Fernández, Licenciada en Periodismo especializada en aspectos de la salud, refiere que los investigadores inyectaron C. albicans directamente en el cerebro de ratones. Tras 4 días se practicó la eutanasia a los animales y se analizaron sus cerebros. Se tomaron imágenes de varios cortes cerebrales y se cultivaron algunas células en placas.
Los resultados, publicados en la revista Cell Reports, sugieren que, una vez en el cerebro, el hongo es capaz de desencadenar 2 mecanismos neuroinmunes para acabar con el intruso.
En el primer mecanismo la enzima fúngica Saps hace que la barrera hematoencefálica sea más permeable. Esto permite que cualquier célula fúngica llegue al cerebro a través del torrente sanguíneo.
Al mismo tiempo, Saps también rompe proteínas similares a la beta amiloide que forman placas en el cerebro con Alzheimer, lo que a su vez activa unas células de limpieza llamadas microglía.
El segundo mecanismo implica otra secreción fúngica, que también activa la microglía, esta vez para eliminar al hongo.
Ambas vías inmunitarias son "muy eficaces para resolver las infecciones agudas por C. albicans", lo que en ratones sanos suelen hacerse en unos 10 días.
Cuando los investigadores interrumpieron intencionadamente la respuesta de la microglía en cerebros de ratón, descubrieron que las infecciones fúngicas se prolongaban mucho más tiempo. Lo que podría pasar en cerebros menos jóvenes y sanos.
"Si eliminamos esta vía, los hongos ya no se eliminan eficazmente en el cerebro", afirma Wu.
Por ahora, se trata sólo de una hipótesis, pero prueba que los péptidos similares a la beta amiloide pueden generarse de una fuente externa como es este hongo.
"Este trabajo aporta potencialmente una nueva pieza importante del rompecabezas en relación con el desarrollo de la enfermedad de Alzheimer", asegura David Corry, Catedrático Fulbright de Patología y profesor de Patología e Inmunología y Medicina en Baylor, autor del estudio.
"La explicación actual de esta enfermedad es que, en su mayor parte, es el resultado de la acumulación de péptidos tóxicos similares a beta amiloide en el cerebro, lo que conduce a la neurodegeneración. La idea dominante es que estos péptidos se producen de forma endógena, nuestras propias proteasas cerebrales descomponen las proteínas precursoras del amiloide generando los péptidos Ab tóxicos".
LUCILA CONTRERAS / CIUDAD CCS








